Schwelend-fortschreitende Multiple Sklerose
Bericht: Felix Schmidtner
* Transparenzhinweis: Die Studie Scalfari et al. 2024 wurde von Sanofi finanziell unterstützt, die Meinungsbildung erfolgte aber unabhängig von den kommerziellen Interessen Sanofis und die Autor:innen sind allein für den Inhalt verantwortlich.
Dank innovativer immunmodulierender und krankheitsmodifizierender Medikamente sind Schübe heute oftmals vermeidbar und Patient:innen, die heute die Diagnose MS erhalten, haben eine deutlich bessere Prognose als jene vor 30 Jahren. Dennoch können kognitive und physische Verschlechterungen auftreten, die mit den traditionellen klinischen Tools und Biomarkern nicht erfasst werden. Scalfari et al. treten daher für eine gemeinsame Definition der schwelend-fortschreitenden Verschlechterung bei MS ein, um die Krankheit besser zu erfassen und den Weg für neue Therapeutika zu ebnen.
Mit der bisherigen Definition von Multipler Sklerose können die Symptome und pathologischen Vorgänge der schwelenden MS nicht erfasst werden, so Scalfari et al. 2024.1 Als Beispiel führen sie den Fall einer 40-jährigen Patientin mit schubförmig remittierender MS (RRMS) an, die mit krankheitsmodifizierenden Therapien so gut therapiert wurde, dass sie seit vier Jahren frei von weiteren Schüben war. Der Score auf der Expanded Disability Status Scale (EDSS-Score) blieb stabil und in der Magnetresonanztomografie (MRT) waren keine neuen oder sich vergrößernden Läsionen sichtbar. Dennoch gab die Patientin in den letzten 18 Monaten an, dass es ihr schlechter gehe, und sie ermüdete schneller nach physischer Aktivität. Nach einer Gehstrecke von 2km wurde ihr – von einem früheren Schub beeinträchtigter rechter Fuß – schlapp. Nach 45 Minuten Gehen musste sie ihre Aktivität komplett einstellen. Zudem klagte sie über „brain fog“ und darüber, dass sie längere Zeit für kognitive Aufgaben brauche.
Dieser Fall mit seiner subtilen, aber für die Patientin ernsten Verschlechterung zeigt die Limitationen der traditionellen Klassifikation der Multiplen Sklerose auf, weshalb Scalfari et al. für das Konzept der schwelend-fortschreitenden Verschlechterung bei MS („smouldering-associated worsening“ – SAW) plädieren. Bei der SAW geht es um eine Progression der Erkrankung unabhängig von Schubaktivität (PIRA), um Gangprobleme und Fatigue, ohne dass verstärkte Läsionen in der Bildgebung sichtbar sind. Für Ao. Univ.-Prof. Dr. Johann Sellner, Primarius der Neurologischen Klinik am Landesklinikum Mistelbach, affiliierte Abteilung der Karl Landsteiner Universität für Gesundheitswissenschaften Krems, hat sich in den letzten Jahren das Verständnis für entzündliche und degenerative Prozesse bei der MS grundlegend verbessert. Bereits in der Frühphase sind zwei unterschiedliche Prozesse für das Auftreten einer bleibenden klinischen Behinderung verantwortlich: die schubabhängige Verschlechterung („relapse-associated worsening“ – RAW) und die PIRA. „Das duale Konzept wird bereits seit vielen Jahren diskutiert, nun liefert eine Expertengruppe Stellungnahmen und Empfehlungen für den Einbezug dieser Erkenntnisse in die klinische Praxis“, erklärt Sellner. Für ihn ist es jedenfalls „ein wichtiger nächster Schritt, dass die schwelende Krankheitsaktivität nicht nur in klinischen Studien berücksichtigt, sondern auch in der individuellen Beurteilung der Patient:innen einbezogen wird. Vor allem die Bruton-Kinase-Inhibitoren (BTKi) könnten die PIRA bremsen, insbesondere jene, die ausreichend die Blut-Liquor-Schranke überschreiten können, so Sellner. Das wäre der fehlende Baustein für eine erfolgreiche Krankheitskontrolle. Im Folgenden stellen wir hier die wichtigsten Punkte aus der Arbeit von Scalfari et al.* von 2024 vor, für die sich 15 MS-Expert:innen aus acht Staaten getroffen haben (im Folgenden als Konsortium bezeichnet), um eine einheitliche Definition dieser schwelenden Verschlechterung der MS, ihrer Pathogenese und ihrer Relevanz für die klinische Praxis zu formulieren.
Klinische Manifestation der schwelenden multiplen Sklerose
Die schwelend-fortschreitende Verschlechterung ist ein Überbegriff, zu dem das Phänomen der PIRA gehört, aber auch andere graduelle Verschlechterungen unabhängig von Schüben, die mit den Standardmessmethoden nicht detektierbar sind. Die Symptome können dabei höchst unterschiedlich sein: subtile motorische Verschlechterungen, kognitive Verlangsamung, Fatigue, neuropathische Schmerzen, Inkontinenz oder sexuelle Dysfunktion.
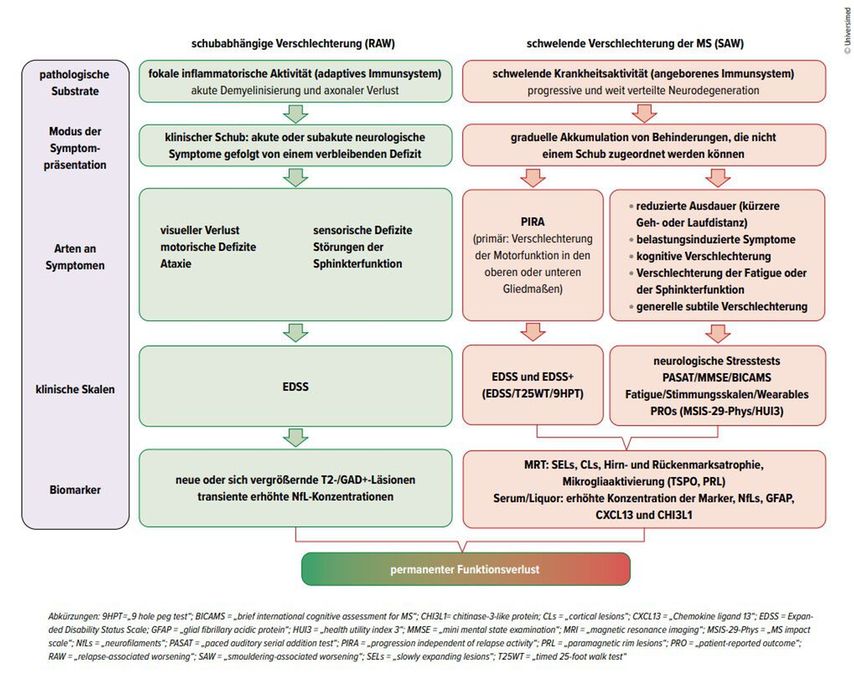
Abb. 1: Schubförmige und sich schwelend verschlechternde Multiple Sklerose im Vergleich (nach Scalfari et al. 2024)1
Pathologische Treiber der schwelenden multiplen Sklerose
Bisher wird eine Kombination aus verbreiteter Entzündung und degenerativer Nervenverletzung, insbesondere axonaler Degeneration, kombiniert mit gescheiterten Kompensationsmechanismen als Ursache für die schwelende multiple Sklerose vermutet.2 Genomweite Assoziationsstudien (GWAS) weisen auf Pathways hin, die beim Zusammenspiel zwischen Neuronen und den unterstützenden Gliazellen beteiligt sind. Bisher konnten aber keine kausalen Mechanismen identifiziert werden. Als Treiber werden folgende pathologische Vorgänge vermutet:
-
chronisch aktive Läsionen mit B-Zell- und T-Zell-Interaktion
-
B-Zell-Aktivierung im ZNS kombiniert mit kortikaler Demyelinisierung
-
von Astrozyten angetriebene chronische Neuroinflammation
-
intrinsische Defizite des neuronalen Stoffwechsels3–5
Zudem ist auffällig, dass bei Patient:innen mit schwelender MS oft eine chronische Entzündung der Meningen vorliegt. Damit verbunden wird eine fokale Verletzung der grauen Substanz beobachtet.
Die Rolle des Alterns bei der schwelend-fortschreitenden multiplen Sklerose
Mit steigendem Alter spielen schwelende Verschlechterungen eine größere Rolle, wobei schwelende Verschlechterungen andererseits auch vorzeitiges Altern bedingen. Es wird vermutet, dass dies in der Ausschöpfung der kognitiven Reserve und dem altersbedingten Rückgang in der Remyelinisierungseffizienz wurzelt. Zudem ist es möglich, dass eine verkürzte Telomerlänge zu epigenetischen Veränderungen und zellulärer Seneszenz führt, die sich ebenfalls als Krankheitsprogression äußern.
Flüssigkeitsbasierte Biomarker für die schwelende Verschlechterung
Für die schwelende Verschlechterung der MS wurden bereits verschiedene blutbasierte und Liquor-Biomarker vorgeschlagen. Dazu gehören die leichten Neurofilamente (NfL) und das saure Gliafaserprotein (GFAP). Das Chitinase-3-like-1-Protein (CHI3L1) wird als CSF-Marker genannt, genauso wie der Chemokin-Ligand 13 (CXCL13).
Die NfL-Konzentration korreliert mit dem neuroaxonalen Verlust, aber auch mit dem Auftreten von Schüben. Zudem ist NfL geeignet, um das Risiko einer PIRA vorherzusagen. GFAP-Konzentrationen steigen mit der Aktivierung von Astrozyten an und können helfen, den Verlust der grauen Substanz vorherzusagen. Dabei ist GFAP als Biomarker unabhängig vom Auftreten weiterer Schübe. Darüber hinaus wird diskutiert, ob GFAP geeignet ist, um zukünftige Behinderungen durch MS vorherzusagen. Kombiniert mit NfL lasse sich gut das Risiko von weiteren Behinderungen und PIRA prognostizieren. CHI3L1-Konzentrationen im Liquor korrelieren mit dem Risiko eines Fortschreitens der Behinderung. CXCL13 ist ein Marker für die Meningitis. Der Ligand kontrolliert zusammen mit seinem Rezeptor CXCR5 die Organisation der B-Zellen in den Lymphfollikeln. Conclusio: Die Autoren sehen GFAP, CXCL13 und CHI3L1 als die vielversprechendsten Biomarker für die schwelende Verschlechterung der MS an.
Bildgebende Biomarker
Um eine schwelende Verschlechterung bildgebend zu erkennen, sind verschiedene Verfahren geeignet. Für das Konsortium ist hier vor allem die Erkennung von langsam expandierenden Läsionen (SEL) und „paramagnetic rim lesions“ (PRL) als Biomarker für chronisch aktive Läsionen relevant.
SEL sind mit konventionellen MRT-Sequenzen erkennbar. Sie zeigen eine größere Gewebedestruktion im Vergleich zu Nicht-SEL-T2-Läsionen und lassen sich mit Magnetisierungstransfer-, Myelinwasser-, Diffusionstensorsequenzen sowie quantitativen T1-Sequenzen erkennen.
PRL lassen sich u.a. mit Single-Echo- und Multi-Echo-Gradienten detektieren. Sie sind im Vergleich zu randlosen T2-Läsionen größer und dehnen sich über die Zeit aus. Vom Konsortium wird das 7Tesla(T)-MRT als Goldstandard bezeichnet, mit 1,5T- oder 3T-MRT sollte die Visualisierung aber auch möglich sein. Die Abklärung von PRL ist jedenfalls von großer Relevanz, weil diese schon in den frühesten Stadien der MS auftreten können und mit schlechteren klinischen und radiologischen Prognosen verbunden sind. Bei Detektion in juxtakortikalen Regionen korreliert das Auftreten einer PRL auch mit der Schwere der kortikalen Demyelinisierung.
PET-Bildgebung
Die Positronenemissionstomografie (PET) ist insbesondere mit dem 18-kDa- Translokator-Protein-PET (TSPO) eine sinnvolle Maßnahme, um die schwelende Entzündung nachzuweisen. Mit TSPO-PET kann die Entzündung sowohl in der normal erscheinenden weißen Substanz als auch in der grauen Substanz quantifiziert werden.
Für die Messung kortikaler Läsionen wird die Verwendung von „neurite-orientation dispersion and density imaging“empfohlen, um die diffusen mikrostrukturellen Abnormalitäten, die hier neurodegenerativ auftauchen, sichtbar zu machen. Das Ausmaß fokaler Demyelinisierung innerhalb der kortikalen und tiefen grauen Substanz korreliert stark mit dem Voranschreiten der Erkrankung. Zudem ist diese Demyelinisierung unabhängig von der Demyelinisierung der weißen Substanz ersichtlich.
Klinische Anzeichen und Integration in die klinische Praxis
Wie das Fallbeispiel aufzeigt, sind klinische Routinetools wie der EDSS-Score nicht immer ausreichend, um die Dynamik der schwelenden Verschlechterung der MS zu erfassen. Mögliche Alternativen, die Verschlechterungen umfangreicher und früher erfassen, sind die Multiple Sclerosis Functional Composite, eine Leistungsskala der US-amerikanischen Multiple-Sklerose-Gesellschaft, und die erweiterte Version der EDSS, die EDSS-Plus. In der Studie von Cadavid et al. 2016 zeigten 59,5% der Patient:innen eine Progression der Behinderung, die mit der EDSS-Plus erfasst wurde, aber nur bei 24,7% wurde sie mit der klassischen EDSS festgestellt.6 Zudem kann die EDSS mit dem 25-Foot-Walk-Test oder dem 9-Hole-Peg-Test noch weitere Aspekte der Verschlechterung erfassen.
Darüber hinaus plädieren die Autor:innen dafür, in Zukunft die neurologische Reserve durch verschiedene Tests wie Geh- und Laufdistanzen bzw. -zeiten, Reaktionszeiten, Gleichgewichtsanalysen und visuelle Tests zu erfassen – in Analogie zu kardiologischen Stresstests. Außerdem müssen diese klinischen und Biomarker-Kriterien auch in klinische Studien implementiert werden, um bedeutende Veränderungen systematisch zu erfassen und relativ zu klinischen Stadien betrachten zu können. Eine Rolle bei der Abschätzung des Einflusses von schwelender Verschlechterung können auch Self-Monitoring-Bögen und „patient-reported outcomes“ (PRO) spielen.
Für die Integration in die klinische Praxis schlägt das Konsortium ein Umdenken vor. Gesundheitspersonal sollte anerkennen, dass sich selbst „klinisch stabile“ Patient:innen mit MS verschlechtern können, und daher hier in der Kommunikation mit den Patient:innen sensibler sein. Schließlich sollte vermieden werden, dass sich Patient:innen ignoriert fühlen und frustriert sind, weil die Verschlechterung nicht gesehen oder anerkannt wird. Die offene Diskussion über die schwelende Verschlechterung bietet zudem die Möglichkeit zum besseren Umgang mit Erwartungen gegenüber den derzeit verfügbaren krankheitsmodifizierenden Therapieoptionen. Angesichts der Tatsache, dass derzeit Medikamente gegen eine schwelende Verschlechterung nicht zur Verfügung stehen, erinnern Scalfari et al. daran, dass die Auswirkungen auch durch einen holistischen Zugang minimiert werden können. Schlechte Gewohnheiten und ungesunde Verhaltensweisen wie Rauchen, wenig Bewegung, ungesunde oder einseitige Ernährung, soziale Isolierung, Einsamkeit und Arbeitslosigkeit gehen mit schlechteren Prognosen einher. Zwar können Mediziner:innen nicht alle Bereiche davon adressieren, aber die Lebensstilfaktoren sollten angesichts ihres Einflusses auf die Auswirkungen der SAW nicht vernachlässigt werden.
Literatur:
1 Scalfari et al.: Smouldering-associated worsening in multiple sclerosis: an international consensus statement on definition, biology, clinical implications, and future directions. Ann Neurol 2024; 96(5): 826-45 2 Kuhlmann T et al.: Multiple sclerosis progression: time for a new mechanism-driven framework. Lancet Neurol 2023; 22: 78-88 3 Trapp BD & Stys PK: Virtual hypoxia and chronic necrosis of demyelinated axons in multiple sclerosis. Lancet Neurol 2009; 8: 280-91 4 De Barcelos IP et al.: Mitochondrial dysfunction and multiple sclerosis. Biology 2019; 8:37 5 Holman SP et al.: Neuronal mitochondrial calcium uniporter deficiency exacerbates axonal injury and suppresses remyelination in mice subjected to experimental autoimmune encephalomyelitis. Exp Neurol 2020; 333: 113430 6 Cadavid D et al.: The EDSS-plus, an improved endpoint for disability progression in secondary progressive multiple sclerosis. Mult Scler 2017; 23: 94-105
Das könnte Sie auch interessieren:
Prognosemarker in der Schlaganfallrehabilitation
In den vergangenen Jahrzehnten sind zahlreiche Publikationen zur frühzeitigen Abschätzung des Rehabilitationserfolges nach Schlaganfall unter Einschluss von klinischen Parametern und ...
Insomnie: Diagnostik, Phänotypen und innovative Therapieansätze
Insomnie zählt zu den häufigsten und hartnäckigsten Schlafstörungen mit erheblichen Folgen für die Lebensqualität. Die umfassende Schlafanamnese und die kognitive Verhaltenstherapie sind ...
Therapie der Epilepsien: aktueller Stand und zukünftige Perspektiven
Leitliniengerechte medikamentöse Therapie unter Berücksichtigung von Epilepsiesyndrom, Alter, Geschlecht und Komorbiditäten stellt den Goldstandard der Epilepsiebehandlung dar. Durch ...